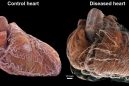
Η χημειοθεραπεία και η θεραπεία με ακτινοβολία προκαλούν μεγάλη νοσηρότητα. Δύο συνταγογραφούμενα φάρμακα, τα Amifostine και Dexrazoxane, και τα δύο αντιοξειδωτικά, μειώνουν τις παρενέργειες της θεραπείας του καρκίνου, χωρίς να την εμποδίζουν να σκοτώνει τους όγκους. Η Amifostine (WR-2721) μειώνει τις παρενέργειες και αυξάνει τα ποσοστά ανταπόκρισης, χωρίς να έρχεται σε σύγκρουση με τη θεραπεία του καρκίνου (1-4). Η Dexrazoxane (ICRF-187) προστατεύει την καρδιά από την τοξικότητα της αδριαμυκίνης, χωρίς να εμποδίζει τις αντιογκικές δράσεις της κάνοντας χήλωση του σιδήρου, που διαφορετικά θα σχημάτιζε ελεύθερες ρίζες (5-6).
Παρά τη συχνή χρήση της Amifostine και της Dexrazoxane και σε αντίθεση με τα επιστημονικά ευρήματα από τη δεκαετία του 1970 σε πολλούς ασθενείς έχουν πει να μην χρησιμοποιούν συμπληρώματα διατροφής με αντιοξειδωτικά και άλλα συστατικά κατά τη διάρκεια της χημειοθεραπείας και/ή της θεραπείας με ακτινοβολία, διότι υπάρχει μια εσφαλμένη αλλά φαινομενικά λογική άποψη ότι τα αντιοξειδωτικά αντιδοτούν την ακτινοβολία και μερικές χημειοθεραπείες, διότι αυτές οι θεραπείες σκοτώνουν παράγοντας ελεύθερες ρίζες, οι οποίες εξουδετερώνονται από τα αντιοξειδωτικά και ότι το φολικό οξύ αντιδοτεί τη μεθοτρεξάτη.
Advertisment
Ορισμένοι ερευνητές υποστηρίζουν ότι τα αντιοξειδωτικά συστατικά μειώνουν το ποσοστό που η χημειοθεραπεία και η ακτινοβολία σκοτώνουν τους όγκους. Υποστηρίζουν ότι οι συμβατικές μέθοδοι προκαλούν οξείδωση και τα αντιοξειδωτικά μειώνουν τη δράση των συμβατικών μεθόδων. Κατά συνέπεια, λένε, δεν θα πρέπει να χορηγούνται αντιοξειδωτικά στους καρκινοπαθείς κατά τη διάρκεια της χημειοθεραπείας και της ακτινοβολίας. Σε απλή χημεία κάποιος μπορεί να σκεφτεί ότι αυτό είναι σωστό. Ωστόσο σε δοκιμαστικούς σωλήνες (in vitro), σε ζώα και σε ανθρώπους καρκινοπαθείς κάτι τέτοιο δεν συμβαίνει. Επειδή ο καρκίνος είναι ένας ιστός στερημένος οξυγόνου ή αναερόβιο κύτταρο, το καρκινικό κύτταρο έχει πολύ φτωχούς μηχανισμούς για απορρόφηση κατάλληλων ποσοτήτων αντιοξειδωτικών. Η εξαίρεση είναι η βιταμίνη C, που είναι παρόμοια στη χημική δομή με τη γλυκόζη, το αγαπημένο καύσιμο για τα καρκινικά κύτταρα.
Σε ένα αναερόβιο περιβάλλον όπως ο καρκίνος τα αντιοξειδωτικά μπορούν να γίνουν οξειδωτικά. Η βιταμίνη C είναι ένας αντικαρκινικός παράγοντας, διότι μοιάζει με το προτιμώμενο καύσιμο του καρκίνου, τη γλυκόζη, και απορροφάται σε αφθονία. Το ασκορβικό οξύ (η βιταμίνη C) σε ένα αναερόβιο περιβάλλον μπορεί να γίνει ένα ισχυρό οξειδωτικό και καταστρέφει το καρκινικό κύτταρο – αλλά μόνο τα καρκινικά κύτταρα, επειδή τα υγιή κύτταρα έχουν μηχανισμούς για απορρόφηση των σωστών ποσοτήτων βιταμίνης C μαζί με τα άλλα αντιοξειδωτικά.
Από τη δεκαετία του 1970 280 in vitro (εργαστηριακές) και in vivo μελέτες, συμπεριλαμβανομένων 50 ανθρώπινων μελετών, έχουν δείξει ότι τα μη συνταγογραφούμενα αντιοξειδωτικά και άλλα συστατικά δεν αντιδοτούν τις θεραπευτικές αγωγές του καρκίνου και ότι μπορούν να ενισχύσουν τις ικανότητές τους να σκοτώνουν τα καρκινικά κύτταρα, μειώνουν τις αρνητικές τους παρενέργειες, προστατεύουν τους φυσιολογικούς ιστούς και σε 15 μελέτες σε ανθρώπους 3.738 ασθενείς είχαν παρατεταμένη επιβίωση.
Advertisment
Η χημειοθεραπεία και η θεραπεία με ακτινοβολία μειώνουν τα επίπεδα των αντιοξειδωτικών στον ορό του αίματος λόγω υπεροξείδωσης των λιπιδίων και ως εκ τούτου προκαλούν υψηλότερο επίπεδο οξειδωτικού στρες. In vitro κυτταρικές μελέτες (7-12) (κοντά στις 100 μελέτες) και μελέτες σε ζώα (13-17) (πάνω από 100) χρησιμοποιώντας συστατικά που περιλαμβάνουν τις βιταμίνες C, A, K, E, D, B6, B12, βήτα-καροτίνη, σελήνιο και κυστεΐνη ως μεμονωμένους παράγοντες ή διδόμενες σε συνδυασμό με χημειοθεραπεία ή tamoxifen ή interferon alpha-2b ή ακτινοβολία ή με συνδυασμούς αυτών των θεραπειών δείχνουν την ίδια επίδραση: Μη αντιδότηση, αυξημένη προστασία των φυσιολογικών ιστών, αυξημένη νέκρωση των όγκων και σε μερικές μελέτες αυξημένη επιβίωση των ζώων.
50 μελέτες σε ανθρώπους που συμπεριέλαβαν 8.521 ασθενείς, σε 5.081 εκ των οποίων δόθηκαν διατροφικά συμπληρώματα, έχουν δείξει ότι τα μη συνταγογραφόμενα αντιοξειδωτικά και άλλα συστατικά:
– δεν αντιδοτούν τις θεραπευτικές αγωγές του καρκίνου
– μπορούν να ενισχύσουν την ικανότητα της θεραπείας να σκοτώσει τα καρκινικά κύτταρα
– μειώνουν τις παρενέργειες της θεραπείας του καρκίνου
– προστατεύουν τους φυσιολογικούς ιστούς από τη θεραπεία του καρκίνου και
– επιμηκύνουν τη ζωή σε 15 μελέτες για 3.738 ασθενείς (18-67).
Το φολικό οξύ δεν αντιδοτεί τη μεθοτρεξάτη (68-69). Οι επιδράσεις της μεθοτρεξάτης, μιας χημειοθεραπείας, μπορούν να ακυρωθούν με φολινικό οξύ, που είναι ένα ανάλογο της βιταμίνης φολικού οξέος. Το φολικό οξύ δεν ακυρώνει τις επιδράσεις της μεθοτρεξάτης. Για να ακυρώσει τις επιδράσεις της μεθοτρεξάτης το φολινικό οξύ πρέπει να δοθεί σε υψηλές δόσεις. Το φολινικό οξύ δεν μπορεί να το πάρει κάποιος από μόνος του, πρέπει να συνταγογραφηθεί.
Ας εξετάσουμε κάποια αντιοξειδωτικά και άλλα θρεπτικά συστατικά.
ΒΙΤΑΜΙΝΗ Κ. Σε μια μελέτη ασθενείς με καρκίνο του στόματος που θεραπεύτηκαν με ενέσεις βιταμίνης Κ3 πριν τη θεραπεία με ακτινοβολία διπλασίασαν τις πιθανότητές τους (20% έναντι 39%) για 5χρονη επιβίωση και για να είναι ελεύθεροι από την ασθένεια (70). Σε κύτταρα λευχαιμίας σε καλλιέργεια, οι βιταμίνες Κ και Ε που προστέθηκαν στα χημειοθεραπευτικά φάρμακα 5FU (fluorouracil) και leucovorin παρείχαν 300% βελτίωση στην αναχαίτιση των όγκων σε σύγκριση με το 5FU μόνο του (71). Ζώα στα οποία δόθηκε μεθοτρεξάτη και Κ3 είχαν βελτιώσεις στην αντιστροφή του καρκίνου χωρίς αύξηση στην τοξικότητα στον ιστό τους (72).
ΒΙΤΑΜΙΝΗ C. Ποντίκια με όγκους στα οποία δόθηκαν υψηλές δόσεις βιταμίνης C μαζί με αδριαμυκίνη είχαν παρατεταμένη ζωή και δεν υπήρξε μείωση στην ικανότητα της αδριαμυκίνης να σκοτώνει τους όγκους (73). Ασθενείς με καρκίνο του πνεύμονα στους οποίους χορηγήθηκαν αντιοξειδωτικά συστατικά πριν, κατά τη διάρκεια και μετά την ακτινοβολία και τη χημειοθεραπεία είχαν αυξημένη καταστροφή των όγκων και σημαντικά μεγαλύτερη διάρκεια ζωής (74).
ΙΧΘΥΕΛΑΙΟ. Ένα λίπος στο ψάρι, το EPA (εικοσαπεντανοϊκό οξύ), βελτιώνει τα αποτελέσματα της υπερθερμίας και της χημειοθεραπείας αλλάζοντας τις μεμβράνες των καρκινικών κυττάρων για αυξημένη ευπάθεια (75).
ΒΙΤΑΜΙΝΗ Α ΚΑΙ ΒΗΤΑ-ΚΑΡΟΤΙΝΗ. Υπάρχει ένα συνεργιστικό όφελος στη χρήση της βιταμίνης Α με καροτενοειδή σε ασθενείς που θεραπεύονται με χημειοθεραπεία, ακτινοβολία και εγχείρηση για κοινές κακοήθειες (76). Η βήτα-καροτίνη και η βιταμίνη Α μαζί παρείχαν σημαντική βελτίωση στο αποτέλεσμα σε ζώα που θεραπεύτηκαν με ακτινοβολία για καρκίνο (77).
ΒΙΤΑΜΙΝΗ Ε. Η έλλειψη βιταμίνης Ε, που είναι συχνή στους καρκινοπαθείς, εντείνει τις καρδιοτοξικές επιδράσεις της αδριαμυκίνης (78). Όσο χειρότερη είναι η έλλειψη της βιταμίνης Ε στα ζώα, τόσο μεγαλύτερη είναι η καρδιακή βλάβη από την αδριαμυκίνη. Τα συμπληρώματα βιταμίνης Ε προλαμβάνουν την παρενέργεια αύξησης της γλυκόζης που προκαλεί το χημειοθεραπευτικό φάρμακο doxorubicin (79). Μια μελέτη βρήκε ότι τα συμπληρώματα βιταμίνης Ε μπόρεσαν να μειώσουν τη νευροτοξικότητα που προκαλεί συχνά η cisplatin (ένα χημειοθεραπευτικό φάρμακο) από το 86% των ασθενών που έπαιρναν placebo και cisplatin στο 31% των ασθενών που έπαιρναν βιταμίνη Ε και cisplatin, που είναι μια μείωση 55%.
ΝΙΑΣΙΝΗ. Τα συμπληρώματα νιασίνης (Β3) σε ζώα ήταν ικανά να μειώνουν την καρδιοτοξικότητα της αδριαμυκίνης, ενώ δεν επενέβαιναν στην ικανότητά της να σκοτώνει τους όγκους (80). Η νιασίνη σε συνδυασμό με ασπιρίνη σε 106 ασθενείς με καρκίνο της ουροδόχου κύστης που έκαναν εγχείρηση και θεραπεία με ακτινοβολία είχαν βελτίωση στην 5χρονη επιβίωση (72% έναντι 27%) σε σύγκριση με την ομάδα ελέγχου (81). Η νιασίνη κάνει τη θεραπεία με ακτινοβολία πιο αποτελεσματική στο να σκοτώνει υποξικά καρκινικά κύτταρα (82).
ΣΕΛΗΝΙΟ. Ζώα με έλλειψη σε σελήνιο έχουν περισσότερη καρδιακή βλάβη από το χημειοθεραπευτικό φάρμακο αδριαμυκίνη (83). Συμπληρώματα σεληνίου και βιταμίνης Ε σε ανθρώπους δεν μείωσαν την αποτελεσματικότητα των χημειοθεραπευτικών φαρμάκων κατά του καρκίνου των ωοθηκών και του τραχήλου (84). Ζώα με μεταμοσχευμένους όγκους που έπειτα θεραπεύτηκαν με σελήνιο και cisplatin είχαν μειωμένη τοξικότητα στο φάρμακο χωρίς αλλαγή στην αντικαρκινική του δράση (85).
ΚΑΡΝΙΤΙΝΗ. Η καρνιτίνη μπορεί να βοηθήσει τον καρκινοπαθή προστατεύοντας την καρδιά από τις βλαπτικές επιδράσεις της αδριαμυκίνης (86).
Photo: Author/Depositphotos
[toggle title="Βιβλιογραφία"]
1. Brizel D.M., Wasserman T.H., Henke M., et al., Phase III randomized trial of amifostine as a radioprotector in head and neck cancer, Journal of Clinical Oncology, 15, 2850-2857, 2000
2. Capizzi R.L., Clinical status and optimal use of Amifostine, Oncology, 13, 1, 47-59, 1999;
3. Dousay L., Mu C., Giarratana M.C., et al., Amifostine improves the antileukemic therapeutic index of mafosfamide: Implications for marrow purging, Blood, 88, 2849-2855, 1995
4. Kemp G., Rose P., Lurain J., et al., Amifostine pretreatment for protection against cyclophosphamide-induced and ciplatin-induced toxicities: results of a randomized control trial in patients with advanced ovarian cancer, Journal of Clinical Oncology, 14, 2101-2112, 1996
5. Hellmann K., Anthracycline cardiotoxicity prevention by dexrazoxane: Breakthrough of a barrier-sharpens antitumor profile and therapeutic index, Journal of Clinical Oncology, 14, 2, 332-333, 1996
6. Swain S.M., Whaley F.S., Gerber M.C., Ewer M.S., et al., Delayed administration of detraxozane provides cardio-protection for patients with advanced breast cancer treated doxorubicin-containing therapy, Journal of Clinical Oncology, 15, 1333-1340, 1997
7. Anderson D., Basaran N., Blowers S.D., Edwards A.J., The effect of antioxidants on bleomycin treatment in in vitro and in vivo genootoxicity assays, Mutat Res, 329, 37-47, 1995
8. Chiang C.D., Song E.J., et al., Ascorbic acid increases accumulation and reverses vincristine resistance of human non-small cell lung cancer cells, Biochem J, 301, 759-764, 1994
9. DeLoecker W., et al., Effects of vitamin C treatment on human tumor cell growth in vitro. Synergism with combined chemotherapy action, Anticancer Res, 13, 103-106, 1993;
10. Miura T., Muraoka S., Ogiso T., Effect of ascorbate on adriamycin-Fe induced lipid peroxidation and DNA damage, Pharmacol Toxicol, 74, 89-94, 1994
11. Prasad K.N., Hernandez C., et al., Modification of the effect of tamoxifen, cisplatin, DTIC, and interferon-alpha 2b on human melanoma cells in culture by a mixture of vitamins, Nutrition and Cancer, 22, 233-245, 1994
12. Vadgama J.V., Wu Y., Shen D., et al., Effect of selenium in combination with adriamycin or taxol on several defferent cancer cells, Anticancer Res, 20, 1391-1414, 2000
13. Ben-Amotz A., et al., Natural beta-carotene and whole body irradiation in rats, Radiat Environ Biophys, 35, 285-288, 1996
14. Bogin E., Marom M., Levi, Changes in serum, liver and kidneys of cisplatin treated rats; Effects of antioxidants, Eur J Clin Chem Clin Biochem, 32, 843-851, 1994
15. El-Nahas S.M., Mattar F.E., Mohamed, Radioprotective effect of vitamins C and E, Mutat Res, 301, 143-147, 1993
16. Kilinc C., Ozcan O., et al., Vitamin E reduces bleomycin-induced lung fibrosis in mice, J Basci Clin Physiol Pharmacol, 4, 249-269, 1993
17. Riabchenko N.I., Ivannik B.P., et al., The molecular, cellular and systemic mechanisms of the radioprotective action of multivitamin antioxidant complexes, Radiats Biol Radioecol, 36, 895-899, 1996
18. Israel L., Hajji O., Greft-Alami A., Desmoulins D., et al., Vitamin A augmentation of the effects of chemotherapy in metastatic breast cancers after menopause. Randomized trial in 100 patients, Annales De Medicine Interne, 136, 7, 551-554, 1985
19. Komiyama S., Kudoh S., Yanagita T., Kuwano M., Synergistic combination of 5FU, vitamin A, and cobalt-60 radiation for head and neck tumors – antitumor combination therapy with vitamin A, Auris, Nasus, Larynx, 12 S2, S239-S243, 1985
20. Meyskens F.L., Kopecky K.J., Phase III randomized trial of the treatment of chronic stage CML with pulse, intermittent busulfan therapy (SWOG 7984): improved survival with the addition of oral vitamin A (50.000 IU/day), Seventh International Conference on the Adjuvant Therapy of Cancer, Tuscon, Arizona, March 10-13, 35, 1993
21. Recchia F., de Filippos S., Rea S., Corrao G., Frati L., Cisplatin, vindesine, 5FU, beta-interferon and retinyl palmitate in advanced non-small cell lung cancer. A phase II study, Proc Annu Meet Am Soc Clin Oncol, 12, A1144, 1993
22. Recchia F., Lelli S., DiMatteo G., Rea S., Frati L., 5FU, cisplatin and retinol palmitate in the management of advanced cancer of the oral cavity. Phase II study, Clin Ter, 142, 5, 403-409, 1993
23. Recchia F., Rea S., Pompili P., Casucci D., Rea M.J., Rizzo F., Gulino A., Frati L., Beta-interferon, retinoids and tamoxifen as maintenance therapy in metastatic breast cancer. A pilot study, Clin Ter, 146, 10, 603-610, 1995
24. Recchia F., Serafini F., Rea S., Frati L., Phase II study of 5FU, folinic acid, epirubicin, mitomycin-C, beta-interferon and retinol palmitate in patients with unresectable pancreatic carcinoma, Proc Annu Meet Am Assoc Cancer Res, 33, A1296, 1992
25. Recchia F., Sica G., de Filippos S., Discepoli S., Rea S., Torchio P., Frati L., Interferon-beta, retinoids, and tamoxifen in the treatment of metastatic breast cancer: a phase II study, J Interferon Cytokine Res, 15, 7, 605-610, 1995
26. Mills E.E.D., The modifying effect of beta-carotene on radiation and chemotherapy induced oral mucositis, Br. J Cancer, 57, 416-417, 1988
27. Santamaria L., Bianchi-Santamaria A., dell’ Orti M., Carotenoids in cancer, mastalgia and AIDS: prevention and treatment – an overview, J Envirn Path, Tox & Oncol, 15, 2-4, 89-95, 1996
28. Besa E.C., Abraham I.L., Bartholomew M.J., Hysninski M., Nowell P.C., Treatment with 13 cis-retinoic acid in transfusion-dependent patients with myelodysplastic syndromes and decreased toxicity with addition of alpha-tocopherol,Am J Med, 89, 739-747, 1990
29. Dimery I., Shirinian M., Heyne K., Lippman S., et al., Reduction in toxicity of high dose 13 cis-retinoic acid with alpha-tocopherol, Proc Annu Meet Am Soc Clin Oncol, 11, A399, 1992
30. Ganser A., Mauer A., Contzen C., Seipelt G., et al., Improved multilineage response of hematopoiesis in patients with myelodysplastic syndromes to a combination therapy with all-trans-retinoic acid, granulocyte colony-stimulating factor, erythropoietin and alpha-tocopherol, Ann Hematol, 72, 4, 237-244, 1996
31. Gottlober P., Krahn G., Korting H.C., Stock W., Peter R.U., The treatment of cutaneous radiation-induced fibrosis with pentoxifylline and vitamin E, Strahlenther Onkol, 172, 1, 34-38, 1996
32. Legha S.S., Wang Y.M., Mackay B., et al., Clinical and pharmacological investigation of the effects of alpha-tocopherol on adriamycin cardiotoxicity, Ann N Y Acad Sci, 393, 411-418, 1982
33. Lenzhofer R., Ganzinger U, Rameis H., Moser K., Acute cardiac toxicity in patients after doxorubicin treatment and the effect of combined tocopherol and nifedipine pretreatment, J Cancer Res Clin Oncol, 106, 143-147, 1983
34. Lopez I., Goudou C., Ribrag V., Sauvage C., Hazebroucq, Dreyfus F., Treatment of mucositis with vitamin E during administration of neutropenic antineoplastic agents, Ann Med Interne, 145, 6, 405-408, 1994
35. Wadleigh R.G., Redman R.S., Graham M.L., Krasnow S.H., Anderson A., Cohen M., Vitamin E in the treatment of chemotherapy induced mucositis, Am J Med, 92, 5, 481-484, 1992
36. Weitzman S.A., Lorell E., Carey R.W., Kaufman S., Stossi T.P., Prospective study of tocopherol prophylaxis for anthracycline cardiac toxicity, Curr Ther Res, 28, 682-686, 1980
37. Wood L.A., Possible prevention of adriamucin-induced alopecia by tocopherol, NEJM, 312, 16, 1060, 1985
38. Copeland E.M. 3rd, MacFadyen B.V. Jr, Lanzotti V.J., Dudrick S.J., Intravenous hyperalimentation as an adjunct to cancer chemotherapy, Am J Surg, 129, 2, 167-173, 1975
39. Filler R.M., Dietz W., Suskind R.M., Jaffe N., Cassady J.R., Parenteral feeding in the management of children with cancer, Cancer, 43 (5 S), 2117-2120, 1979
40. Jaakkola K., Lahteenmaki P., Laaksa J., Harju E., et al., Treatment with antioxidants and other nutrients in combination with chemotherapy, irradiation in patients with small cell lung cancer, Anticancer Res, 12, 3, 599-606, 1992
41. Lockwood K., Moesgaard S., Hanioka T., Folkers K., Apparent partial remission of breast cancer in “high risk” patients supplemented with nutritional antioxidants, essential fatty acids and coenzyme Q10, Mol Asspects Med, 15 Suppl: 231-240, 1994
42. Osaki T., Ueta E., Yoneda K., Hirota J., Yamamoto T., Prophylaxis of oral mucositis associated with chemoradiotherapy for oral carcinoma by Azelastine with other antioxidants, Head Neck, 16, 4, 331-339, 1994
43. Pyrhonen S. Kuitunen T., Nyandoto P., Kouri M., Randomized comparison of fluorouracil, epidoxorubicin and methotrexate (FEMTX) plus supportive care with supportive care alone in patients with non-resectable gastric cancer, Br. J Cancer, 71, 3, 587-591, 1995
44. Rougereau A., Sallerin T., Chapet J., Robin J.C., Rougereau G., Adjuvant treatment of patients with neoplastic lesions using the combination of a vitamin complex and an amino acid. Apropos of a series of 17 cases of epidermoid carcinoma of the upper aerodigestive tract, Ann Gastroenterol Hepatol, 29, 2, 99-102, 1993
45. Sakamoto A., Chougule P.B., Prasad K.N., Retrospective analysis of the effect of vitamin A, C, and E in human neoplasms, in: Medulation and Mediation of Cancer by Vitamins. Karger, Basel, 330-333, 1983
46. Thiruvengadam R., Kaneshiro C., Iyer P., Slater L., Kurosaki T., Effect of antioxidant vitamins and mineral on chemotherapy induced cytopenia, Proc Annu Meet Am Soc Clin Oncol, 15, A1793, 1996
47. Wagdi P., Rouvinez G., Fluri M., Aeschbacher B., Thoni A., Schefer H., Meier B., Cardioprotection in chemo- and radiotherapy for malignant diseases – an echocardiographic pilot, Schweiz Rundsch Med Prax, 84, 43, 1220-1223, 1995
48. Kim J.H., He S.Q., Dragovic J., et al., Use of vitamins as adjunct to conventional cancer therapy, in: Nutrients in Cancer Prevention and Treatment, Prasad K.N., Santamaria L., Williams R.M., eds, Humana Press, 363-372, 1995
49. Ladner H.A., Salkeld R.M., Vitamin B6 status in cancer patients: effects of tumour site, irradiation, hormones and chemotherapy, in: Nutrition, Growth, and Cancer, Alan R. Liss, 273-281, 1988
50. Wiernik P.H., Yeap B., Vogl S.E., Kaplan B.H., Comis R.L., et al., Hexamethylmelamine and low or moderate dose cisplatin with or without pyridoxine for the treatment of advanced ovarian carcinoma: a study of the Eastern Cooperative Oncology Group, Cancer Invest, 10, 1, 1-9, 1992
51. DeRosa L., Montuoro A., DeLaurenzi A., Therapy of ‘high risk’ myelodysplastic syndromes with an association of low dose Ara-C, retinoic acid and 1,25 dihydroxyvitamin D3, Biomed Pharmacoth, 46, 5-7, 211-217, 1992
52. Margolin K.A., Akman S.A., Leong L.A., Morgan R.J., Somlo G., et al., Phase I study of mitomycin C and menadione in advanced solid tumors, Cancer Chemother Pharmacol, 36, 4, 293-298, 1995
53. Nagoumey, et al., Menadiol in combination with cytotoxic chemotherapies: feasibility for resistance modification, Proc Ann Meet Am Soc Clin Oncol, 6, A132, 1987
54. Bohm S., Oriana S., Spatti G., et al., Dose intensification of platinum compounds with glutathione protection as induction chemotherapy for advanced ovarian carcinoma, Oncology, 57, 2, 115-120, 1999
55. Bohm S., Battista Spatti G., Di Re F., Oriana S., Pilotti S., Tedeschi M., Tongella S., Zunino F., A feasibility study of cisplatin administration with low-volume hydration and glutathione protection in the treatment of ovarian carcinoma, Anticancer Res, 11, 4, 1613-1616, 1991
56. Cascinu S., Cordella L., Del Ferro E., Fronzoni M., Catalano G., Neuroprotective effect of reduced glutathione on cisplatin-based chemotherapy in advanced gastric cancer: a randomized double-blind placebo-controlled trial, J Clin Oncol, 13, 1, 26-32, 1995
57. Cozzaglio L., Doci R., Colella G., et al., A feasibility study of high-dose cisplatin and 5-fluorouracil with glutathione protection in the treatment of advanced colorectal cancer, Tumori, 76, 6, 590-594, 1990
58. Di Re F., Bohm S., Oriana S., Spatti G.B., Pirovano C., Tedeschi M., Zunino F., High-dose cisplatin and cyclophosphamide with glutathione in the treatment of advanced ovarian cancer, Ann Oncol, 4, 1, 55-61, 1993
59. Di Re F., Bohm S., Oriana S., Spatti G.B., Zunino F., Efficacy and safety of high-dose cisplatin and cyclophosphamide with glutathione protection in the treatment of bulky advanced epithelial ovarian cancer, Cancer Chemother Pharmacol, 25, 5, 355-360, 1990
60. Fontanelli R., Spatti G., Raspagliesi F., Zunino F, Di Re F., A preoperative single course of high-dose cisplatin and bleomycin with glutathione protection in bulky stage IB/II carcinoma of the cervix, Ann Oncol, 3, 2, 117-121, 1992
61. Leone R., Fracasso M.E., Soresi E., et al., Influence of glutathione administration on the disposition of free and total platinum in patients after administration of cisplatin, Cancer Chemother Pharma, 29, 5, 385-390, 1992
62. Locatelli M.C., D’ Antona A., Labianca R., et al., A phase II study of combination chemotherapy in advanced ovarian carcinoma with cisplatin and cyclophosphamide plus reduced glutathione as potential protective agent against cisplatin toxicity, Tumori, 79, 1, 37-39, 1993
63. Nobile M.T., Vidili M.G., Benasso M., et al., A preliminary clinical study of cyclophosphamide with reduced glutathione as uro-protector, Tumori, 75, 3, 257-258, 1989
64. Oriana S., Bohm S., Spatti G., Zunino F., Di Re F., A clinical experience with reduced glutathione as protector against cisplatin-toxicity, Tumori, 73, 337-340, 1987
65. Parnis F.X., Coleman R.E., Harper P.G., et al., A randomised double-blind controlled clinical trial assessing the tolerability and efficacy of glutathione as an adjuvant to escalating doses of cisplatin in the treatment of advanced ovarian cancer, Eur J Cancer, 31A, 10, 1721, 1995
66. Plaxe S., Freddo J., Kim S., et al., Phase I trial of cisplatin in combination with glutathione, Gynecol Oncol, 55, 1, 82-86, 1994
67. Smyth J.F., Bowman A., Perren T., et al., Glutathione reduces the toxicity and improves quality of life of women diagnosed with ovarian cancer treated with cisplatin: results of a double-blind, randomised trial, Ann Oncol., 8, 6, 569-573, 1997
68. Leeb B.F., Folic acid and cyanocobalamin levels in serum and erythrocytes during low-doses methotrexate therapy of reumatoid arthritis and psoriatic arthritic patients, Clin Exp Rheum, 13, 459-463, 1995
69. Morgan S.L., Baggott J.E., Vaughn W.H., Austin J.S., Veitch T.A., Lee J.Y., et al., Supplementation with folic acid during methotrexate therapy for rheumatoid arthritis. A double blind, placebo-controlled trial, Ann Intern Med, 121, 11, 833-841, 1994
70. Krishanamurthi S., et al., Radiology, 99, 409, 1971
71. Waxman S., et al., Eur. J. Cancer Clin. Oncol., 18, 685, 1982
72. Gold J., Cancer Treatment Reports, 70, 1433, Dec. 1986
73. Shimpo K., Am J Clin Nutr, 54, 1298S, 1991
74. Jaakkola K., Anticancer Res, 12, 599, 1992
75. Burns C.P., et al., Nutrition Reviews, 48, 233, June 1990
76. Santamaria L., et al., Nutrients and cancer prevention, 299, 1990
77. Seifter E., et al., J Nat Cancer Inst, 71, 409, 1983
78. Signal P.K., et al., Mol Cell Biochem, 84, 163, 1988
79. Geetha A., et al., J Biosci, 14, 243, 1989
80. Schmitt-Graff A., et al., Pathol Res Pract, 181, 168, 1986
81. Popov A.I., Med Radiol, 32, 42, 1987
82. Kjellen E., et al., Radiotherapy Oncology, 22, 81, 1991
83. Coudray C., et al., Basic Res Cardiol, 87, 173, 1992
84. Sundstrom H., et al., Carcinogenesis, 10, 273, 1989
85. Okhawa K., et al., Br J Cancer, 58, 38, 1988
86. Furitano G., et al., Drugs Exp Clin Res, 10, 107, 1984
[/toggle]
- Τα συμπληρώματα διατροφής με αντιοξειδωτικά δεν αντιδοτούν τη χημειοθεραπεία και την ακτινοβολία - 12 Σεπτεμβρίου 2017
- Αντιμετωπίστε την ψωρίαση με διατροφή, βιταμίνες και βότανα - 24 Μαρτίου 2016
- Πώς σχηματίζονται οι χολόλιθοι: Διαλύστε τους με φυσικές μεθόδους - 11 Ιανουαρίου 2016